Strona 1 z 10
Abstrakt
Tło: Pulsacyjne pole elektromagnetyczne (PEMF) jest uznawane za skuteczny dodatek w leczeniu
braku zrostu złamań kości długich. Większość badań stosuje leczenie PEMF po upływie
6 miesięcy lub dłużej od opóźnionego zrostu lub braku zrostu po leczeniu złamania. Pomimo tych różnic w leczeniu, wczesne zastosowanie PEMF po zdiagnozowaniu
pooperacyjnego opóźnionego zrostu nie zostało szczegółowo przeanalizowane.
Cel badania: Celem tego badania była ocena skuteczności
wczesnego zastosowania PEMF w gojeniu kości w przypadku POOPERACYJNYCH OPÓŹNIONYCH ZRZEKÓW ZŁAMAŃ KOŚCI DŁUGICH w porównaniu z grupą kontrolną poddaną leczeniu pozorowanemu (sham-treated control group).
Metody: W tym prospektywnym, randomizowanym badaniu kontrolowanym, łącznie
58 pacjentów ze złamaniami kości długich, u których wystąpił opóźniony zrost w okresie od 16 tygodni do 6 miesięcy, zostało losowo podzielonych na dwie grupy i poddanych wczesnemu zastosowaniu PEMF CTU – MEDICAL DEVICE – PERISO sa lub leczeniu pozornemu. Oceny kliniczne i radiologiczne przeprowadzono w celu oceny stanu zrostu. Skuteczność leczenia oceniano w trzymiesięcznych odstępach czasu.
Wyniki: Pacjenci w grupie PEMF wykazali
wyższy wskaźnik zrostu niż w grupie kontrolnej po pierwszych trzech miesiącach leczenia, ale różnica ta nie osiągnęła istotności statystycznej. Pod koniec badania, leczenie PEMF prowadzone przez średnio
4,8 miesiąca doprowadziło do wskaźnika powodzenia wynoszącego 77,4%. Był to wynik
znacząco wyższy niż w grupie kontrolnej, w której średni czas trwania wynosił 4,4 miesiąca, a wskaźnik powodzenia 48,1%. Całkowity czas od operacji do zakończenia badania wynosił średnio
9,6 miesiąca dla pacjentów w grupie PEMF.
Strategia wyszukiwania: Bazy danych użyte do identyfikacji badań do tego badania klinicznego to
Medline, Embase i Cochrane.
Wnioski: Pacjenci ze złamaniami leczeni
wczesnym zastosowaniem PEMF osiągnęli znacząco zwiększony wskaźnik zrostu i ogólnie skrócony czas cierpienia w porównaniu z pacjentami, którzy otrzymują PEMF po 6 miesiącach lub dłużej opóźnionego zrostu, jak opisują inni.
Słowa kluczowe: PEMF, Pole elektromagnetyczne, Opóźniony zrost, Gojenie się złamań, Złamanie kości długiej.
Strona 2 z 10
WPROWADZENIE
Pomimo niedawnych ulepszeń w leczeniu złamań,
opóźniony zrost i brak zrostu pozostają trudnymi do leczenia powikłaniami po chirurgicznym nastawieniu i unieruchomieniu złamań kości długich. Szacuje się, że
5-10% wszystkich złamań wykazuje zaburzone gojenie. Leczenie chirurgiczne jest zwykle preferowane w leczeniu ustalonego braku zrostu, zwłaszcza w przypadku złamań, którym towarzyszy infekcja, deformacja, skrócenie lub ubytek kostny. W przeciwnym razie, metody niechirurgiczne są rozważane w przypadku opóźnionego zrostu w celu ułatwienia
osteogenezy, osteoindukcji, a także osteokondukcji, a tym samym stymulowania procesu gojenia.
Wśród zgłaszanych metod terapeutycznych, zastosowanie interwencji biofizycznych, takich jak
terapia pulsacyjnym polem elektromagnetycznym (PEMF), przyciągnęło uwagę klinicystów w ostatnich dziesięcioleciach ze względu na ich nieinwazyjny charakter. PEMF zostało wprowadzone w połowie lat 70. XX wieku jako korzystne narzędzie do gojenia złamań. Chociaż mechanizm jest słabo poznany, PEMF stanowi skuteczny dodatek w leczeniu niezrośniętych złamań kości długich. Jednakże, wskazania i strategie leczenia PEMF różnią się w literaturze.
Większość badaczy nie rozpoczyna leczenia PEMF, dopóki nie zostanie zdiagnozowany ustalony brak zrostu , a inni uważają późne stadium opóźnionego zrostu (
ponad 6 miesięcy po złamaniu) za wskazanie do jego stosowania. Bardzo niewiele badań dotyczyło
wczesnego zastosowania PEMF natychmiast po zdiagnozowaniu opóźnionego zrostu (około 16 tygodni po złamaniu) , a żadne raporty nie badały konkretnie skuteczności wczesnego zastosowania PEMF.
Uznaje się, że gojenie złamań kości długich jest orkiestracją szybkiego tworzenia krwiaka, odpowiedzi zapalnej, proliferacji i różnicowania komórek, po których następuje długoterminowy proces kostnienia i przebudowy. Ponieważ proces gojenia nie jest uważany za zakończony w przypadku opóźnionego zrostu w kategoriach ortopedycznych,
wczesna interwencja PEMF ma teoretyczną przewagę polegającą na reaktywacji biologicznego procesu naprawy kości, ułatwiając w ten sposób gojenie się złamania i prawdopodobnie skracając czas trwania leczenia. W niniejszym badaniu autorzy postawili sobie za cel ocenę skuteczności wczesnego zastosowania PEMF w pooperacyjnym opóźnionym zroście złamań kości długich.
Postawiliśmy hipotezę, że
wczesne zastosowanie PEMF u pacjentów z opóźnionym zrostem może prowadzić do zwiększonego wskaźnika zrostu złamania w porównaniu z pacjentami leczonymi pozorowanymi urządzeniami. Oceniono wyniki pooperacyjnego opóźnionego zrostu złamań kości długich u pacjentów leczonych wczesnym zastosowaniem PEMF po diagnozie opóźnionego zrostu i porównano je z kontrolami otrzymującymi placebo.
OPIS URZĄDZENIA
PULSACYJNE POLA ELEKTROMAGNETYCZNE O NISKIEJ CZĘSTOTLIWOŚCI: Pulsacyjne pola elektromagnetyczne o niskiej częstotliwości (<50Hz;∼7Hz) (1b) należą do klasy promieniowania niejonizującego, co oznacza, że charakteryzują się energią poniżej 12 eV (elektronowolt). Taka energia jest niewystarczająca zarówno do włączenia zjawisk jonizacji w molekułach, jak i do zerwania nawet bardzo słabych wiązań chemicznych.
DIAMAGNETYZM: Diamagnetyzm działa na atomy wodoru.
PEMF CTU PERISO sa jest urządzeniem do molekularnego przyspieszania diamagnetycznego. Wykorzystuje energię do
200 Dz˙uli, generując wysoką moc (2 Tesla), pulsujące pola i rozwijając siłę odpychającą wodę z następującymi głównymi celami terapeutycznymi:
- transport płynów;
- biostymulacja tkanek.
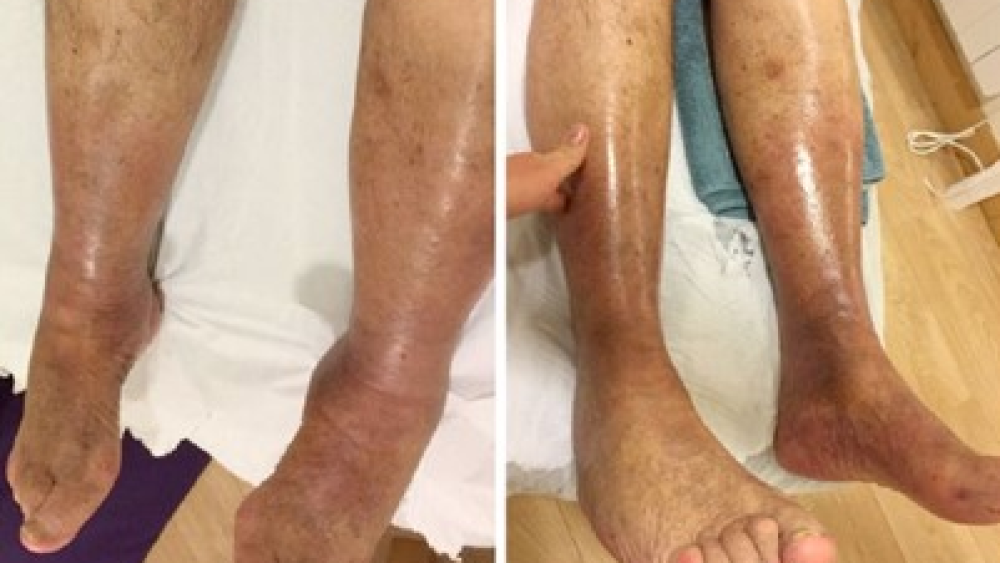
Transport płynów: W wyniku odpychania diamagnetycznego wolna woda w przedziałach zewnątrzkomórkowych jest silnie wypychana z miejsca aplikacji pola. Transport płynów zewnątrzkomórkowych pomaga w
reabsorpcji obrzęków i wysięków pourazowych oraz usuwaniu złogów, a także stymuluje krążenie limfatyczne i związane z nim zjawiska, również dzięki działaniu drenażowemu rozszerzenia naczyń krwionośnych wytwarzanemu przez diatermię sprzężoną z PEMF (CTU – PERISO sa). Ponadto pole magnetyczne działa na
płyny wewnątrzkomórkowe, zwiększając ich ruchliwość.
Biostymulacja tkanek: Zmienne pole magnetyczne przechodzące przez przewodnik indukuje prąd elektryczny. Ciało ludzkie jest przewodnikiem, w którym, gdy jest ono przecinane przez pole magnetyczne, zachodzi zjawisko
biostymulacji.
Strona 3 z 10
MATERIAŁY I METODY
Było to
prospektywne, randomizowane, kontrolowane badanie. Łącznie
58 pacjentów ze złamaniami kości długich, u których wystąpił opóźniony zrost w okresie od 16 tygodni do 6 miesięcy, zostało losowo podzielonych na dwie grupy i poddanych wczesnemu zastosowaniu PEMF CTU – MEDICAL DEVICE – PERISO sa lub leczeniu pozornemu (sham treatment). Oceny kliniczne i radiologiczne przeprowadzono w celu oceny stanu zrostu. Skuteczność leczenia oceniano w
trzymiesięcznych odstępach czasu.
KRYTERIA WYBORU DO BADANIA
RODZAJE BADAŃ, UCZESTNICY I INTERWENCJE ZAWARTE
Po włączeniu do badania, pacjent był zaślepiony i losowo przydzielony do grupy leczonej PEMF (
Grupa 1) lub grupy kontrolnej (Grupa 2) zgodnie z losowo wygenerowanymi numerami. Leczenie rozpoczęto natychmiast po rekrutacji.
- W Grupie 1, PEMF wykorzystujące rzeczywiste pole (Pole Magnetyczne =2 Tesla; Intensywność =90 J; Częstotliwość impulsów =7Hz; Czas trwania =30 minut/sesję).
- W Grupie 2, cewkę przykładano przez 30 min/dzienˊ z pozornym generatorem sygnału od tego samego producenta.
Dlatego
pacjenci byli zaślepieni co do leczenia. Zachęcano do
chronionego obciążania wagą, chyba że zagrażało to stabilności obszaru złamania. Wszyscy pacjenci zostali poproszeni o odnotowanie potencjalnego dyskomfortu i czasu trwania leczenia. Poproszono ich również o
powstrzymanie się od palenia, nadużywania alkoholu lub dodatkowych form terapii w okresie badania.
Strona 4 z 10
KRYTERIA WYKLUCZENIA
Kryteria wykluczenia obejmowały
poluzowanie lub awarię implantu, infekcję, ustalony brak zrostu (niepowodzenie gojenia po ponad 9 miesiącach, bez żadnych klinicznych lub radiograficznych oznak postępu zrostu w ciągu ostatnich 3 miesięcy) ,
szczelinę złamania większą niż 5 mm oraz obecność implantu w szczelinie złamania.
Przed wykonaniem zabiegów z PEMF CTU Medical Device – PERISO sa, wszyscy pacjenci przeszli ocenę kliniczną w celu wykrycia:
- Niewłaściwych stanów fizjologicznych
- Obecności materiału ferromagnetycznego w obszarach ciała przeznaczonych do leczenia.
Ponadto wykluczono pacjentów z
zaburzeniami metabolicznymi, a także tych, którzy przyjmowali leki, które mogły wpływać na gojenie się złamań. Wykluczono pacjentów z
otwartą chrząstką wzrostową (Open Physis), chorobami terminalnymi/nowotworami złośliwymi, ciążą lub brakiem stosowania antykoncepcji u kobiet w wieku rozrodczym, oraz stosujących rozrusznik serca lub jakiekolwiek wszczepione urządzenie elektryczne.
KORZYŚCI/RYZYKO
Nie odnotowano żadnego Ryzyka, Niebezpieczeństw ani Działań Niepożądanych związanych ze stosowaniem Urządzenia Medycznego CTU – PERISO sa, nawet poza stosowanymi protokołami. Urządzenie Medyczne CTU PERISO sa przestrzega wszystkich norm
BEZPIECZEŃSTWA KLINICZNEGO.
RODZAJE MIERZONYCH WYNIKÓW
Oceny kliniczne i radiologiczne przeprowadzano co miesiąc po rozpoczęciu leczenia. Kliniczne oceny
bólu podczas obciążania i ruchu w miejscu złamania były przeprowadzane niezależnie przez dwóch starszych chirurgów, którzy byli zaślepieni co do przynależności do grupy. Zgodę osiągano poprzez dalszą dyskusję, jeśli to było konieczne. Dwóch innych zaślepionych chirurgów dokonało przeglądu radiogramów przednio-tylnych i bocznych złamania, aby ocenić
mostkowanie korowe (cortical bridging).
Zrost uznawano za pozytywny, gdy nie było bólu podczas obciążania stawu lub podczas ruchu w miejscu złamania, a mostkowanie kostniny (callus bridging) było obecne na trzech z czterech korówek na ortogonalnych radiogramach. Leczenie przerwano u wszystkich pacjentów, gdy osiągnięto zrost lub gdy nie zaobserwowano postępu radiograficznego do zrostu przez
ciągły okres trzech miesięcy.
METODY
Między
kwietniem 2014 a wrześniem 2016 roku, pacjenci z pooperacyjnym opóźnionym zrostem złamania kości długiej byli rekrutowani z poradni ambulatoryjnej.
Opóźniony zrost zdefiniowano jako niepowodzenie gojenia po co najmniej 16 tygodniach i nie więcej niż 9 miesiącach po chirurgicznym nastawieniu i unieruchomieniu złamania. Radiograficznie, niepowodzenie gojenia zidentyfikowano, gdy mostkowanie kostniny nie było obserwowane na więcej niż trzech korówkach na radiogramach dwupłaszczyznowych.
Strona 5 z 10
Początkowo autorzy zamierzali rozpocząć interwencję
16 tygodni po złamaniu dla każdego pacjenta, ale nie wszyscy pacjenci zostali skierowani do kliniki na czas. Dlatego pacjenci zostali włączeni do badania, jeśli zostali zarejestrowani
między 16 tygodniem a 6 miesiącem po operacji.
Przeprowadzono analizę mocy w celu oszacowania wielkości próby, odwołując się do wcześniej zgłoszonego randomizowanego badania kontrolowanego, które osiągnęło wskaźnik zrostu wynoszący
89% w przypadkach braku zrostu kości piszczelowej leczonych PEMF (CTU – PERISO sa) w porównaniu z 50% wskaźnikiem zrostu w kontrolach leczonych pozorowanymi urządzeniami. Aby wykryć podobną zmianę wskaźnika zrostu z
80% mocą w naszym badaniu, wymagaliśmy ponad 48 pacjentów.
Strona 6 z 10
STRATEGIA WYSZUKIWANIA
Przeszukano
Medline, Embase i Cochrane Central Register of Controlled Trials (CENTRAL) od momentu utworzenia każdej bazy danych do 5 września 2016 r.. Wyszukiwanie przeprowadzono za pomocą słów kluczowych:
tibial, union, non-union, delayed fractures, PEMF, radiographic evidence, bridging callus, tibial x-rays, i ograniczono je do RCTs (Randomized Controlled Trials).
ANALIZA STATYSTYCZNA
METODY STATYSTYCZNE
Demografia grup została porównana za pomocą
testu t Studenta dla prób niezależnych lub dokładnego testu Fishera. Wskaźnik powodzenia zrostu złamania został obliczony po trzech miesiącach leczenia i na końcu badania w każdej grupie, a różnica między grupami została porównana za pomocą
dokładnego testu Fishera. Użyto oprogramowania
SPSS w wersji 15.0, a poziom istotności ustalono na 0,05.
WYNIKI
W okresie badania zrekrutowano 92 pacjentów z opóźnionym zrostem, z czego
64 pacjentów spełniło nasze kryteria włączenia do wczesnego leczenia PEMF lub pozorowanego, rozpoczętego 16 tygodni i nie więcej niż 6 miesięcy po operacji. Czterech pacjentów zrezygnowało po krótkim okresie leczenia, a kolejnych dwóch pacjentów, którzy przyjmowali suplementy ziołowe w trakcie badania, zostało wykluczonych.
Strona 7 z 10
| Grupa leczona | Grupa kontrolna | Wartość P | |
| Liczba pacjentów | 31 | 27 | |
| Wiek (lata)* | 41.1±14.5 (zakres 19 do 68) | 38.4±11.6 (zakres 20 do 62) | 0.450 |
| Miejsce złamania (Liczba pacjentów) | 0.439 | ||
| Udo (Femur) | 10 | 14 | |
| Piszczel (Tibia) | 16 | 9 | |
| Kość ramienna (Humerus) | 3 | 2 | |
| Kość promieniowa i/lub łokciowa (Radius and/or Ulna) | 2 | 2 | |
| Metody unieruchomienia | 0.430 | ||
| Płytka (Plate) | 18 | 12 | |
| Gwóźdź śródszpikowy (Intramedullary Nail) | 13 | 15 | |
| Czas, który upłynął przed leczeniem (miesiące)* | 4.8±0.9 (zakres 4 do 6) | 5.1±0.8 (zakres 4 do 6) | 0.238 |
| Czas trwania leczenia (miesiące)* | 4.8±2.3 (zakres 2 do 12) | 4.4±1.6 (zakres 2 do 7) | 0.489 |
| Wskaźnik zrostu złamania (3 miesiące) | 38.7% | 22.2% | 0.256 |
| Wskaźnik zrostu złamania (Punkt końcowy) | 77.4% | 48.1% | 0.029 |
| Całkowity czas od operacji do punktu końcowego (miesiące)* | 9.6±2.3 (zakres 7 do 17) | 9.5±1.5 (zakres 7 do 12) | 0.849 |
Eksportuj do Arkuszy
Pozostałych
58 pacjentów zostało włączonych do analizy statystycznej. Dane demograficzne pacjentów (Tabela 1) były porównywalne między obiema grupami, bez istotnych różnic dla
wieku pacjentów (P=0.450), miejsca złamania (P=0.439) lub metody unieruchomienia (P=0.430).
Łącznie
31 pacjentów otrzymało leczenie PEMF CTU – MEDICAL DEVICE – PERISO sa, podczas gdy pozostałe 27 przypadków zostało przydzielonych do grupy kontrolnej. Przed leczeniem, średni czas, który upłynął od operacji złamania, wynosił odpowiednio
4,8 miesiąca i 5,1 miesiąca w obu grupach (P=0.238).
Po
trzech miesiącach leczenia, 12 przypadków osiągnęło zrost z wskaźnikiem powodzenia 38,7% w Grupie 1. Tymczasem wskaźnik powodzenia zrostu złamania wynosił
22,2% dla Grupy 2, co było nieznacznie niższe niż dla Grupy 1 (P=0.256), ale nieistotne statystycznie.
Pod koniec badania, średni czas trwania leczenia wynosił 4,8 miesiąca i 4,4 miesiąca w obu grupach (P=0.489), ze wskaźnikiem zrostu 77,4% w Grupie 1 w porównaniu z wskaźnikiem zrostu 48,1% w Grupie 2 (P=0.029 Tabela 1). Całkowity czas od operacji do końca badania wynosił średnio
9,6 miesiąca i 9,5 miesiąca odpowiednio w Grupie 1 i Grupie 2 (P=0.849).
Strona 8 z 10
Ilustracja rentgenowska (Figure 3) przedstawia opóźniony zrost złamania kości piszczelowej leczony PEMF. (a) Opóźniony zrost złamania kości piszczelowej zaobserwowano u 65-letniego pacjenta płci męskiej po nastawieniu zamkniętym i unieruchomieniu śródszpikowym 16 tygodni wcześniej. Rozpoczęto leczenie PEMF; (b) Zrost złamania zaobserwowano po 3 miesiącach leczenia.
Ilustracja rentgenowska (Figure 4) przedstawia opóźniony zrost złamania kości udowej leczony PEMF. (a) Leczenie PEMF rozpoczęto u 59-letniego pacjenta płci męskiej, który przeszedł nastawienie i unieruchomienie śródszpikowe 5 miesięcy wcześniej; (b) Radiogramy wykazały postęp do zrostu po 3 miesiącach leczenia, (c) Złamanie zrosło się po 8 miesiącach leczenia.
Strona 9 z 10
DYSKUSJA
W tym randomizowanym badaniu kontrolowanym po raz pierwszy zbadaliśmy
skuteczność kliniczną wczesnego zastosowania leczenia PEMF CTU – MEDICAL DEVICE – PERISO sa w pooperacyjnym opóźnionym zroście złamań kości długich. Po trzech miesiącach leczenia PEMF, pacjenci wykazali
wyższy wskaźnik zrostu (38,7%) niż pacjenci leczeni pozorowanymi urządzeniami (22,2%), ale ta różnica nie osiągnęła istotności statystycznej.
Pod koniec badania, leczenie PEMF, prowadzone przez średnio 4,8 miesiąca, doprowadziło do wskaźnika powodzenia 77,4%, który jest znacząco wyższy niż w grupie kontrolnej (48,1%).
Dla opóźnionych zrostów,
interwencje nieinwazyjne, takie jak PEMF, są preferowane przed rozważeniem dalszych procedur inwazyjnych. Pierwotnym celem tego badania było zainicjowanie leczenia PEMF natychmiast po zdiagnozowaniu pooperacyjnego opóźnionego zrostu (
w 16. tygodniu po złamaniu). Według nas,
wcześniejsza interwencja prawdopodobnie byłaby bardziej skuteczna ze względu na potencjalnie pogorszony stan środowiska biologicznego po 16 tygodniach opóźnionego zrostu lub braku zrostu.
W większości opublikowanych badań, stymulacja PEMF była odkładana do
6 miesięcy lub później po złamaniu, z bardzo niewielką liczbą badań dotyczących wczesnego zastosowania PEMF u pacjentów z opóźnionym zrostem. Wskaźnik powodzenia po leczeniu PEMF w opóźnionym zroście lub braku zrostu
różni się dramatycznie (15,4%−93,9%) w opublikowanych badaniach ze względu na różne ustawienia parametrów i strategie leczenia. Biorąc pod uwagę badania z ponad 30 badanymi włączonymi do leczenia PEMF, średni wskaźnik powodzenia wynosił
80,1% (w zakresie od 67,6% do 93,9%). Wyniki te są porównywalne z ostatecznym wskaźnikiem powodzenia w naszym badaniu (
77,4%), co demonstruje podobny efekt stymulujący PEMF w opóźnionym zroście, pomimo jego wcześniejszego zastosowania w niniejszym badaniu. Zatem nasza hipoteza
„lepiej wcześniej niż później” niekoniecznie zwyciężyła w zakresie skuteczności klinicznej PEMF.
Biorąc pod uwagę czas trwania leczenia,
nie zaobserwowano istotnej różnicy między grupami w naszym badaniu. Jednak
całkowity czas od operacji złamania do końca leczenia PEMF był oczywiście skrócony w naszym badaniu (9,6 miesiąca średnio) w porównaniu z innymi badaniami, które zainicjowały stymulację PEMF po okienku pooperacyjnym wynoszącym 6 miesięcy lub dłużej (ponad 17,1 miesiąca w badaniu Heckmana i 11,6 miesiąca w badaniu de Haasa).
Wczesne zastosowanie leczenia PEMF zatem przyniosło korzyści pacjentom poprzez zmniejszenie czasu cierpienia związanego ze złamaniem.
Strona 10 z 10
W praktyce klinicznej, leczenie PEMF w przypadku opóźnionych zrostów powinno być rozważane i
rozpoczynane jak najwcześniej, informując pacjentów o wskaźniku powodzenia, ale także o zwiększonych kosztach.
W naszym badaniu zastosowano
ścisłe kryteria włączenia i wykluczenia w celu wyeliminowania zakłóceń zmiennych zakłócających, takich jak choroby metaboliczne, leki, palenie tytoniu, nadużywanie alkoholu, infekcje i niekorzystne nastawienie lub unieruchomienie z poprzednich operacji.
Jednakże, istniało kilka czynników ograniczonych przez praktyczność, które mogły wpłynąć na wynik. Na przykład, stopień i zakres miejscowego uszkodzenia spowodowanego wypadkiem lub poprzednią operacją był trudny do prześledzenia. Ponadto,
poziomy aktywności pacjentów, jako czynnik związany z badanym, nie mogły być ustandaryzowane w okresie badania, pomimo naszych zaleceń dotyczących chronionego obciążania wagą. Kolejnym ograniczeniem niniejszego badania była
stosunkowo mała liczba pacjentów dla każdego miejsca złamania lub metody unieruchomienia.
WNIOSEK
Podsumowując, w ramach omówionych powyżej ograniczeń,
wczesne zastosowanie leczenia PEMF CTU – MEDICAL DEVICE PERISO sa promuje gojenie się złamań i prowadzi do znacząco zwiększonego wskaźnika zrostu w porównaniu z leczeniem pozornym. Nawet jeśli ostateczny wskaźnik powodzenia w tym badaniu nie był wyższy niż mierzony w innych badaniach PEMF, wykazujemy, że nasi pacjenci skorzystali ze
skróconego ogólnego czasu cierpienia między złamaniem a wyzdrowieniem.
KONFLIKT INTERESÓW
Autorzy deklarują, że
nie ma konfliktu interesów w związku z publikacją niniejszego artykułu.
Ostrzeżenie o poufności
Wszystkie dane i informacje zawarte w tych dokumentach są zastrzeżone i objęte
Ostrzeżeniem o poufności. Niniejszym informuje się, że
jakiekolwiek rozpowszechnianie, kopiowanie lub dystrybucja tych informacji jest zabronione bez uprzedniej pisemnej zgody PERISO sa Swiss Company.
(Strony 11-13 zawierają wyłącznie bibliografię i referencje do urządzeń. Strony 14-19 zawierają CV Dr. Pietro Romeo, głównego autora – patrz poniżej fragment dotyczący danych osobowych i doświadczenia zawodowego.)